國(guó)家(jiā)藥品不(bù)良反應監測年(nián)度報(bào)告 (2023年(nián))
為(wèi)全面反映2023年(nián)我國(guó)藥品不(bù)良反應監測情況,提高(gāo)安全用(yòng)藥水(shuǐ)平,更好(hǎo)地(dì)保障公衆£用(yòng)藥安全,國(guó)家(jiā)藥品不(bù)良反應監測中心組織編撰《國(guó)家(jiā)藥品不(bù)良γ反應監測年(nián)度報(bào)告(2023年(nián))》。
第1章(zhāng) 藥品不(bù)良反應監測工(gōng)作(zuò)情況
2023年(nián),國(guó)家(jiā)藥品不(bù)良反應監測中心在國(guó)家(jiā)藥品監督管理(lǐ)局的(de)領導下(xià),全面貫徹¶黨的(de)二十大(dà)精神,認真落實“四個(gè)最嚴”要(yào)求,按照(zhào)“講政治、強監管、保安全、促發展、惠民(mínΩ)生(shēng)”的(de)工(gōng)作(zuò)思路(lù),紮實有(yǒu)效開(kāi)展各項工(gōng)作(zuò),為(wèi)藥品監管提供科(kē )學有(yǒu)力支撐,切實保護和(hé)促進公衆健康。
一(yī)是(shì)體(tǐ)系能(néng)力建設縱深推進。貫徹落實《國(guó)務院辦公廳關于全面加強藥品監管能(néng)力建設的(de)實施意見(jiàn)》《“十四五”國(guó)家(jiā)藥品安全及促進高(gāo)質量發展規劃》,加強對(duì)基層監測機(jī)構和(hé)醫(yī)療機(jī∑)構指導,督促藥品上(shàng)市(shì)許可(kě)持有(yǒu)人(rén)(以下(xià)簡稱“持有(y©ǒu)人(rén)”)落實主體(tǐ)責任,持續強化(huà)“一(yī)體(tǐ)兩翼”工(gōng)作(zuò)格局。
二是(shì)法規制(zhì)度體(tǐ)系更加完善。配合推進《藥品不(bù)良反應報(bào)告和(hé)監測管理(lǐ)辦法》修訂,研究起草(cǎo)《非處方藥轉換為(wèi)處方藥工(gōng)作(zuò)程序》等技(jì)術(βshù)指南(nán)和(hé)規範性文(wén)件(jiàn),指導持有(yǒu)人(rén)開(kāi)展藥物(wù)警戒工(gōng)作(zuò),推動藥物(wù)警戒制(zαhì)度建立健全。
三是(shì)安全風(fēng)險防控不(bù)斷加強。密切關注國(guó)內(nèi)外(wài)監管動态,強化(huà)監測數(shù)據分(fēn)析評價。完成36個(gè)(類)藥品安全性評價,提出風(fēng)險控制(zhì)措施建議(yì),國(guó)家(jiā)藥♥監局發布修訂藥品說(shuō)明(míng)書(shū)公告34期。
四是(shì)監測信息系統持續優化(huà)。加強基礎設施建設,擴容基礎環境,增加網絡安全防護能(néng)力。重構藥品不(bù)良反應監測系統,推進創新藥和(hé)附條件(jiàn)批準藥品不(bù)良反應術(shù±)語提取信息化(huà)建設,為(wèi)監測評價提供有(yǒu)效技(jì)術(shù)支撐。
五是(shì)監管科(kē)學研究深入實施。加強與科(kē)研院所、高(gāo)等院校(xiào)、醫(yī)療機(jī)構合作(zuò),完成監¥管科(kē)學行(xíng)動計(jì)劃第二批重點項目研究。加強重點實驗室建設與課題研究,合作(zuò)開(kāi)展國(guó)家(jiā)自(zì)然科(kē)學基金(jīnπ)、科(kē)技(jì)部重大(dà)專項課題申報(bào)與研究。
第2章(zhāng) 藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告情況
2.1 報(bào)告總體(tǐ)情況
2.1.1 2023年(nián)度藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告情況
2023年(nián)全國(guó)藥品不(bù)良反應監測網絡收到(dào)《藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告表》241.9萬份。1÷999年(nián)至2023年(nián),全國(guó)藥品不(bù)良反應監測網絡累計(jì)收到(dào)《藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告表》2,3α27.5萬份(圖1)。
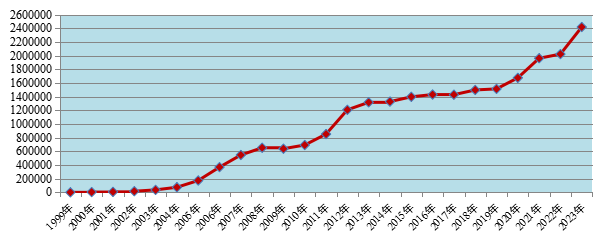
圖1 1999年(nián)-2023年(nián)全國(guó)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告數(shù)量增☆長(cháng)趨勢
2.1.2 新的(de)和(hé)嚴重藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告情況
2023年(nián)全國(guó)藥品不(bù)良反應監測網絡收到(dào)新的(de)和(hé)嚴重藥品不(bù)良反應/事(shì)件(jiàn)報≥(bào)告83.3萬份;新的(de)和(hé)嚴重藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告占同期報(bào)告總數(shù)的(de)34.5%。
2023年(nián)全國(guó)藥品不(bù)良反應監測網絡收到(dào)嚴重藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告37.8萬份,嚴重藥品不(bù)良反應/事×(shì)件(jiàn)報(bào)告占同期報(bào)告總數(shù)的(de)15.6%(圖2)。
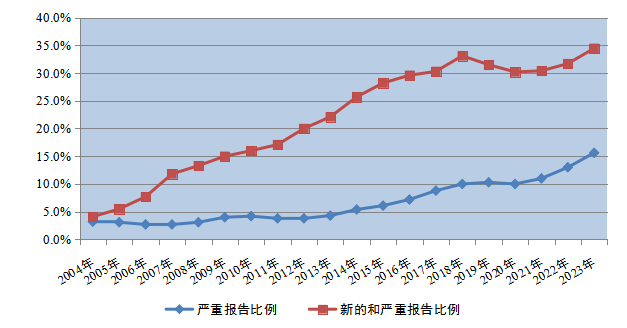
圖2 20042023年(nián)新的(de)和(hé)嚴重以及嚴重藥品不(bù)良反應/事(sh₩ì)件(jiàn)報(bào)告比例
小(xiǎo)貼士:
如(rú)何正确認識藥品不(bù)良反應報(bào)告?
藥品不(bù)良反應是(shì)指合格藥品在正常用(yòng)法用(yòng)量下(xià)出現(xiàn)的(de)與用(yòπng)藥目的(de)無關的(de)有(yǒu)害反應。藥品不(bù)良反應是(shì)藥品的(de)固有(yǒu)屬性,一(yī)般來(lái)說₩(shuō),所有(yǒu)藥品都(dōu)會(huì)存在或多(duō)或少(shǎo)、或輕或重的(de)不(bù)良¥反應。
藥品不(bù)良反應監測是(shì)藥品上(shàng)市(shì)後安全監管的(de)重要(yào)支撐,其目的(de)是(shì)及 時(shí)發現(xiàn)和(hé)控制(zhì)藥品安全風(fēng)險。持有(yǒu)人(rén)、經營企業(yè)、醫(yī)療機(jī)構應當報(bào)告所發現(xiàn)α的(de)藥品不(bù)良反應,國(guó)家(jiā)鼓勵公民(mín)、法人(rén)和(hé)其他(tā)組織報(bào)告藥品不(bù)良反應。
經過各方努力,持有(yǒu)人(rén)、經營企業(yè)、醫(yī)療機(jī)構報(bào)告藥品不←(bù)良反應的(de)積極性已經逐步提高(gāo),我國(guó)藥品不(bù)良反應報(bào)告數(shù)量穩步增長(™cháng),與歐盟、美(měi)國(guó)等國(guó)家(jiā)和(hé)地(dì)區(qū)藥品不(bù)良反應報(bào)告數(shù)量發展趨勢相(xiàng)同。嚴重藥品不(bù)良"反應/事(shì)件(jiàn)報(bào)告比例是(shì)衡量報(bào)告總體(tǐ)質量和(hé)可(kě)利用(yòng)性的(de)重要(yào)指标之一(yī),藥品不(bù)良反應→監測評價工(gōng)作(zuò)一(yī)直将收集和(hé)評價新的(de)和(hé)嚴重藥品不(bù)良反應作(zuò)為(wèi←)重點內(nèi)容。新的(de)和(hé)嚴重藥品不(bù)良反應報(bào)告,尤其是(shì)嚴重藥品不(bù)良反應報(bào)告數(shù)量增多(duō),并非說(shuō)明®(míng)藥品安全水(shuǐ)平下(xià)降,而是(shì)意味著(zhe)監管部門(mén)掌握的(de)信息越來(lái)越全面,對(du£ì)藥品的(de)風(fēng)險更了(le)解,風(fēng)險更可(kě)控,對(duì)藥品的(de)評價更加有(yǒu)依據,監管決•策更加準确。同樣,在醫(yī)療實踐中,能(néng)及時(shí)了(le)解藥品不(bù)良反應發生(shēng)∑的(de)表現(xiàn)、程度,并最大(dà)限度地(dì)加以避免,也(yě)是(shì)保證患者用(yòng)藥安全的(de)重要(yào)措施。
2.1.3 每百萬人(rén)口平均報(bào)告情況
每百萬人(rén)口平均報(bào)告數(shù)量是(shì)衡量一(yī)個(gè)國(guó)家(jiā)藥品不•(bù)良反應監測工(gōng)作(zuò)水(shuǐ)平的(de)重要(yào)指标之一(yī)。2023年(nián)我國(guó)每百萬人(rén)口平均報(bào)告數(shù)為(wèi)1,716份。
2.1.4 藥品不(bù)良反應/事(shì)件(jiàn)縣級報(bào)告比例
藥品不(bù)良反應/事(shì)件(jiàn)縣級報(bào)告比例是(shì)衡量我國(guó)藥品不(bù)良反應監測工(g↑ōng)作(zuò)均衡發展及覆蓋程度的(de)重要(yào)指标之一(yī)。2023年(nián)全國(guó)98.5%的(de)縣級地(dì)區(qū)報(bào)告φ了(le)藥品不(bù)良反應/事(shì)件(jiàn)。
2.1.5 藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告來(lái)源
持有(yǒu)人(rén)、經營企業(yè)和(hé)醫(yī)療機(jī)構是(shì)藥品不(bù)良反應報(bào)告的(de)責任單位。按照(zhào)報(bào)告來(lái)源統計(πjì),2023年(nián)來(lái)自(zì)醫(yī)療機(jī)構的(de)報(bào)告占90.1%、來(l→ái)自(zì)經營企業(yè)的(de)報(bào)告占6.3%、來(lái)自(zì)持有(yǒ¥u)人(rén)的(de)報(bào)告占3.5%、來(lái)自(zì)其他(tā)報(bào)告者的(de✘)報(bào)告占0.1%(圖3)。
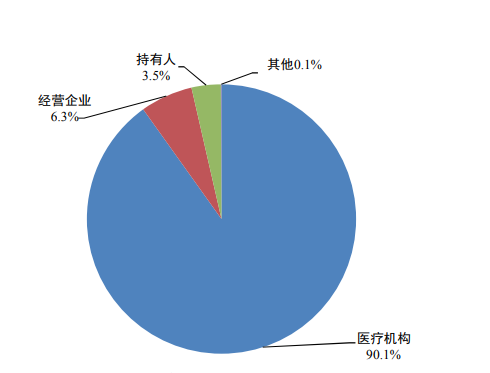
圖3 2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告來(lái)源
按照(zhào)報(bào)告數(shù)量統計(jì),2023年(nián)持有(yǒu)人(rén)報(bào)送藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告共γ計(jì)8.5萬份,同比增長(cháng)0.8%。其中,新的(de)和(hé)嚴重藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告占持有(yǒu)人(rén)報(bào)告總數(✔shù)的(de)51.9%,高(gāo)于總體(tǐ)報(bào)告中新的(de)和(hé)嚴重藥品不(bù)良反應>/事(shì)件(jiàn)報(bào)告占比。
2.1.6 報(bào)告人(rén)職業(yè)
按照(zhào)報(bào)告人(rén)職業(yè)統計(jì),醫(yī)生(shēng)占56.8%、藥師(shī)占25.7%、護士占12.5%、其他(tā)職業(yè)占5.0%(圖4)。
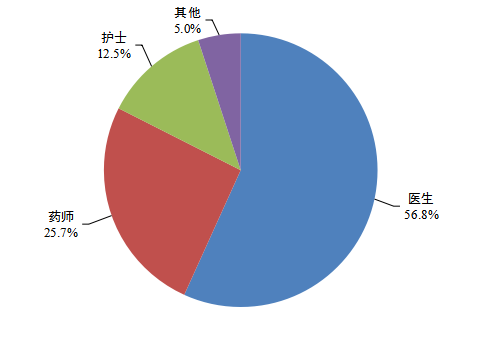
圖4 2023年(nián)報(bào)告人(rén)職業(yè)構成
2.1.7 藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及患者情況
2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,女(nǚ)性多(duō)于男(nán¥)性,男(nán)女(nǚ)性别比為(wèi)0.84:1。從(cóng)年(nián)齡分(fēn)布看(kàn),14歲及以下(xià)兒(ér)童患者占8.4%,65歲及以上(shàng)老(lǎo)年(nián)患者占33.1%(圖5)。
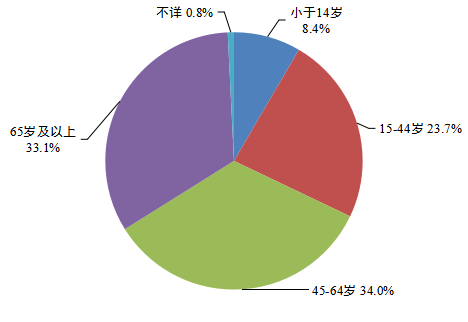
圖5 2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及患者年(nián)齡
2.1.8 藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及藥品情況
按照(zhào)懷疑藥品類别統計(jì),化(huà)學藥品占81.2%、中藥占12.6%、生(shēng)物(wù)制(zhì)品占3.8%、無法分(fēn)類占2.4%(圖6)。
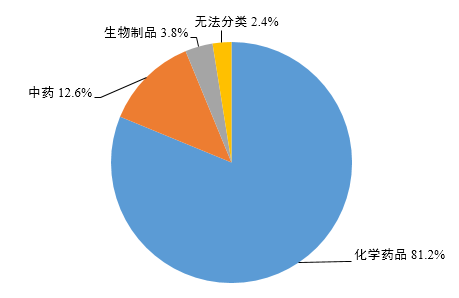
圖6 2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及藥品類别
按照(zhào)給藥途徑統計(jì),2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射給藥占56.3%、口服給 藥占34.4%、其他(tā)給藥途徑占9.3%;注射給藥中,靜(jìng)脈注射給藥占91.1%、其他(tā)注射給藥占8.9%(圖7)。
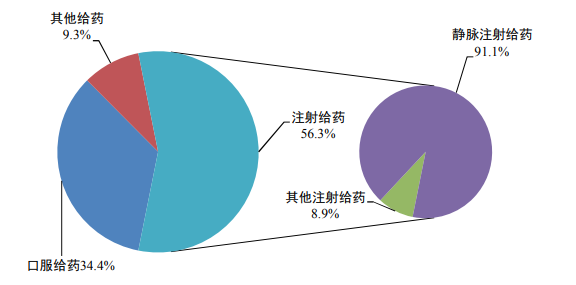
圖7 2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及給藥途徑
2.1.9 藥品不(bù)良反應/事(shì)件(jiàn)累及器(qì)官系統情況
2023年(nián)報(bào)告的(de)藥品不(bù)良反應/事(shì)件(jiàn)中,累及器(qì)官系統排名前3位依次為(wèi)胃腸系統疾病、皮膚及皮下(xià)組織類疾病↔、全身(shēn)性疾病及給藥部位各種反應(圖8)。
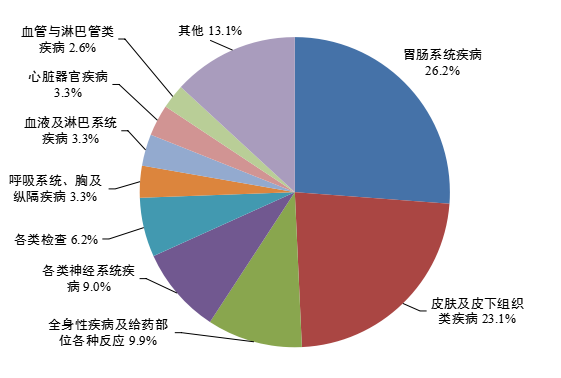
圖8 2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)累及器(qì)官系統
2.2 化(huà)學藥品、生(shēng)物(wù)制(zhì)品監測情況
2.2.1 總體(tǐ)情況
2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,涉及懷疑藥品262.7萬例次,其中化(huà)學藥品占81.2%,生(shēng)物(wù₽)制(zhì)品占3.8%。2023年(nián)嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及懷疑藥品47.9萬例次,其中化(huà)學藥品占84.9%,生(shē♣ng)物(wù)制(zhì)品占6.7%。
2.2.2 涉及患者情況
2023年(nián)化(huà)學藥品、生(shēng)物(wù)制(zhì)品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,男(nán)女(nǚ)患者比為(wèi)0.85:γ1,女(nǚ)性多(duō)于男(nán)性。14歲以下(xià)兒(ér)童患者的(de)報(bào)告占8.8%,65歲及以上(shàng)老(lǎo)年(nián)患者的♦(de)報(bào)告占33.4%。
2.2.3 涉及藥品情況
2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及的(de)化(huà)學藥品中,例次數(shù)排名前5位的(de)類别依次為(wèi)抗感染藥、腫瘤用(×yòng)藥、心血管系統用(yòng)藥、鎮痛藥、電(diàn)解質/酸堿平衡及營養藥。2023年(nián)嚴重藥品不(bù)良≥反應/事(shì)件(jiàn)涉及化(huà)學藥品中,報(bào)告數(shù)量最多(duō)的(de)"為(wèi)腫瘤用(yòng)藥,占32.8%;其次是(shì)抗感染藥,占30.7%。
2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及的(de)生(shēng)物(wù)制(zhì)品中,細胞因子(zǐ↑)占68.2%、抗毒素及免疫血清占9.0%、血液制(zhì)品占4.0%、診斷用(yòng)生(shēng)物(wù)制(zhì)品占0.3%。
按劑型統計(jì),2023年(nián)化(huà)學藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑、口服制(zhì)劑✘所占比例分(fēn)别為(wèi)60.8%和(hé)32.9%,其他(tā)劑型占6.3%。生(shēng)物(wù)制(zhì)品中,注射劑、口 服制(zhì)劑占比分(fēn)别為(wèi)80.1%和(hé)1.2%,其他(tā)制(zhì)劑(含不(bù)詳)占18. 7%。
2.2.4 總體(tǐ)情況分(fēn)析
2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告情況與2022年(nián)相(xiàng)比未出現(xiàn)顯著變化(huà)。從(cóng)不(b≤ù)良反應涉及患者年(nián)齡看(kàn),14歲以下(xià)兒(ér)童占比出現(xiàn)小(xiǎo)幅上(shàng)α升,但(dàn)總體(tǐ)安全性依然良好(hǎo);65歲及以上(shàng)老(lǎo)年(nián)患者占比仍然保持升高(gāo)趨勢,提示臨•床應持續加強對(duì)老(lǎo)年(nián)患者的(de)安全用(yòng)藥管理(lǐ)。從(cóng)化(huβà)學藥品類别上(shàng)看(kàn),抗感染藥報(bào)告數(shù)量仍居于首位,其占比在連續多(d¥uō)年(nián)下(xià)降後首次出現(xiàn)上(shàng)升情況,且莫西(xī)沙星和(hé)阿奇黴素報(bào)告數(shù)量出現(xiàn)較大(dà)幅度上(s₽hàng)升,考慮與2023年(nián)呼吸道(dào)感染性疾病高(gāo)發有(yǒu)關。生(shēng)物(w∏ù)制(zhì)品中排名前五位的(de)藥品仍以大(dà)分(fēn)子(zǐ)單克隆抗體(tǐ)類抗腫瘤藥居多(duō),與2022年(nián)±相(xiàng)比信迪利單抗、利妥昔單抗的(de)報(bào)告數(shù)量增幅相(xiàng)對(duì)較大(dà)。
小(xiǎo)貼士:
什(shén)麽是(shì)喹諾酮類藥品,使用(yòng)時(shí)應注意什(shén)麽?
喹諾酮類藥品是(shì)目前臨床常用(yòng)的(de)抗菌藥物(wù),包括左氧氟沙星、莫西(xī)沙星、加替沙星、環丙沙星、氟羅沙★星、諾氟沙星等。此類藥物(wù)抗菌譜廣,治療領域寬,臨床用(yòng)量大(dà),不(bù)良反應也(yě)倍受關注。喹諾酮類藥品口服或注射均可(kě)産生(shē ng)胃腸道(dào)反應,如(rú)惡心、嘔吐、腹痛、腹瀉等。因其可(kě)通(tōng)過血腦(nǎo)屏障,還(hái)可(kě)引起中樞神經系統不(bù)良反應,如(rú)興奮、失眠☆、頭痛、頭暈、椎體(tǐ)外(wài)系反應、幻覺等,嚴重者出現(xiàn)癫痫大(dà)發作(zuò)、精神分(fēn)裂樣反應、∏意識障礙等,臨床使用(yòng)時(shí)應加強對(duì)神經系統不(bù)良反應的(de)監測。此÷類藥物(wù)還(hái)可(kě)能(néng)影(yǐng)響血糖水(shuǐ)平,出現(xiàn)低(dī)血糖、↓高(gāo)血糖等血糖異常變化(huà),糖尿病患者使用(yòng)應當格外(wài)注意。喹諾酮類藥物(wù)在尿液中溶解度降低(dī)可(kě)析&出結晶,引起結晶尿、血尿,嚴重者可(kě)導緻急性腎功能(néng)衰竭,故服藥期間(jiān)應多(duō)飲水(shuǐ),每日(rì)進水(shuǐ)量應•在1200 ml以上(shàng)。一(yī)些(xiē)喹諾酮類還(hái)可(kě)出現(xiàn)光(guāng)敏反應,如(rú)司帕沙星,使用(yòngγ)藥物(wù)後暴露于紫外(wài)線可(kě)能(néng)發生(shēng)皮膚癢感、紅(hóng)斑、水(shuǐ)腫、水(shuǐ)泡等症狀,用(yòng)藥期間(jiān¥)應注意避光(guāng)。喹諾酮類藥品的(de)其他(tā)嚴重風(fēng)險,如(rú)肌腱炎和(hé)肌腱斷裂、周圍神經病變、主動脈瘤和(hé)主動脈夾層等,請(qǐng)參見(j€iàn)國(guó)家(jiā)藥監局發布的(de)《藥品不(bù)良反應信息通(tōng)報(bào)》和(hé)藥品說(shuō) 明(míng)書(shū)修訂公告。
2.3 中藥監測情況
2.3.1 總體(tǐ)情況
2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,涉及懷疑藥品262.7萬例次,其中中藥占12.6%;2023年(nián)嚴重不(₩bù)良反應/事(shì)件(jiàn)報(bào)告涉及懷疑藥品47.9萬例次,其中中藥占5.4%。
2.3.2 涉及患者情況
2023年(nián)中藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,男(nán)女(nǚ)患者比為(wèi)0.8:1,女(nǚ)性多(duō)于男(©nán)性。14歲及以下(xià)兒(ér)童患者占6.4%,65歲及以上(shàng)老(lǎo)年(nián)患者占31.0%。
2.3.3 涉及藥品情況
2023年(nián)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告涉及的(de)中藥中,例次數(shù$)排名前5位的(de)類别分(fēn)别是(shì)理(lǐ)血劑中活血化(huà)瘀藥(20.3%)、清熱(rè)劑中清熱(rè)解毒藥(1ε3.0%)、祛濕劑中清熱(rè)除濕藥(7.0%)、祛濕劑中祛風(fēng)勝濕藥(4.3%)、補益劑中益氣養陰藥∏(3.9%)。2023年(nián)中藥嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告的(de)例次 數(shù)排名前5位的(de)類别分(fēn)别是(shì)理(lǐ)血劑中活血化(huà)瘀藥(31.2%)、清熱(rè)劑中清熱(rè)解毒藥(11.5%)、補益劑中益氣養陰藥(8.α3%)、開(kāi)竅劑中涼開(kāi)藥(7.1%)、祛濕劑中清熱(rè)除濕藥(4.6%)。
2023年(nián)中藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑和(hé)口服制(zhì)劑所占比例分(fēn→)别為(wèi)25.9%和(hé)60.6%。
2.3.4 總體(tǐ)情況分(fēn)析
與2022年(nián)相(xiàng)比,2023年(nián)中藥不(bù)良反應/事(shì)件(δjiàn)報(bào)告數(shù)增長(cháng)率為(wèi)17.5%,嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告占比為(wèi)7.6%,低(dī)≠于總體(tǐ)藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告占比。從(cón€g)藥品類别上(shàng)看(kàn),活血化(huà)瘀藥的(de)報(bào)告數(shù)量依然居首位,但(dàn)占比略有(yǒu)下(xià)降。從(cóng)總體(tǐ)情況看(kà©n),2023年(nián)中藥占總體(tǐ)不(bù)良反應/事(shì)件(jiàn)報(bào)告比例呈下(xià)降趨勢,但(dàn)仍需≠要(yào)注意安全用(yòng)藥。
小(xiǎo)貼士:
為(wèi)什(shén)麽中藥會(huì)引起不(bù)良反應?
“是(shì)藥三分(fēn)毒”,中藥和(hé)其他(tā)藥品一(yī)樣,在發揮治療作(zuò)用(yòng)的(de)同時(shí),也(yě)可(kě)能(néng)會☆(huì)産生(shēng)一(yī)定不(bù)良反應。辨證論治是(shì)中醫(yī)認識疾病和(hé)治療疾病的(de)基本原則,嚴格→按照(zhào)說(shuō)明(míng)書(shū)規定的(de)功能(néng)主治使用(yòng)中藥♥,有(yǒu)助于減少(shǎo)和(hé)避免不(bù)良反應/事(shì)件(jiàn)的(de)發生(shēng)。如(rú)果不(bù)遵循中醫(yī)辨證論治的(de) 原則或者辨證不(bù)當、超說(shuō)明(míng)書(shū)功能(néng)主治用(yòng)藥,可(kě)能(néng)增加中藥不(bù)良反應/事(shì)件(jiàn)發生(shēn↔g)風(fēng)險。随著(zhe)中藥臨床使用(yòng)日(rì)趨廣泛,應提高(gāo)中藥安全使用(yòng)意識。
2.4 基本藥物(wù)監測情況
2.4.1 國(guó)家(jiā)基本藥物(wù)監測總體(tǐ)情況
2023年(nián)全國(guó)藥品不(bù)良反應監測網絡共收到(dào)《國(guó)家(jiā)基本藥物(wù)目錄(2018年(ni≤án)版)》收載品種的(de)不(bù)良反應/事(shì)件(jiàn)報(bào)告111.2萬份,其中嚴重報(bào)告18.9萬份,占17."0%。報(bào)告涉及化(huà)學藥品和(hé)生(shēng)物(wù)制(zhì)品占87.9%,中成藥占12.1%$。
2.4.2 國(guó)家(jiā)基本藥物(wù)化(huà)學藥品和(hé)生(shēng)物(wù)制(zhì)品情況₹分(fēn)析
《國(guó)家(jiā)基本藥物(wù)目錄(2018年(nián)版)》化(huà)學藥品和(hé)生(shēng)物(wù)制(zhì)品部分(fēn)共417個(gè)(類)品種。2023年(nián)全國(guó)藥品不(bù★)良反應監測網絡共收到(dào)國(guó)家(jiā)基本藥物(wù)化(huà)學藥品和(hé)生(shēng)物(wù)制(zhì)品藥品不(bù)良反應/事(shì)件(jiàn€)報(bào)告105.2萬例次,其中嚴重報(bào)告21.6萬例次,占20.5%。
2023年(nián)國(guó)家(jiā)基本藥物(wù)化(huà)學藥品和(hé)生(shēng)物(wù)制(zhì)品↕不(bù)良反應/事(shì)件(jiàn)報(bào)告按照(zhào)藥品類别統計(jì),報(bào)告數(shù)量排名前5位的(de)分(fēn)别是(shì)抗≤微(wēi)生(shēng)物(wù)藥、抗腫瘤藥、心血管系統用(yòng)藥、激素及影(yǐng)響內(nèi)分(fēn)泌藥、治療精神障礙藥;累及器(qì)官系統排名前5位的(®de)是(shì)胃腸系統疾病、皮膚及皮下(xià)組織類疾病、各類神經系統疾病、全身(shēn)性疾病及給藥部位各種反應、各類檢查。
2.4.3 國(guó)家(jiā)基本藥物(wù)中成藥情況分(fēn)析
《國(guó)家(jiā)基本藥物(wù)目錄(2018年(nián)版)》中成藥共涉及268個(gè)品種。2023年(nián)全國(guó)藥品不(bù)良反應監測網絡收到(dào)國(gu±ó)家(jiā)基本藥物(wù)中成藥不(bù)良反應/事(shì)件(jiàn)報(bào)告14.4萬例次,其中嚴重的(de)不(bù)良反應/事(shì)→件(jiàn)報(bào)告11,504例次,占8.0%。2023年(nián)國(guó)家(jiā)基©本藥物(wù)7大(dà)類中成藥中,藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告ε總數(shù)由多(duō)到(dào)少(shǎo)依次為(wèi)內(nèi)科(kē)用(yòng)藥、骨傷科(kē)用(yòng)藥、婦科(✘kē)用(yòng)藥、外(wài)科(kē)用(yòng)藥、耳鼻喉科(kē)用(yòng)藥、兒(ér)科(kē)用(yòng)藥、眼科(k←ē)用(yòng)藥。
監測數(shù)據表明(míng),2023年(nián)國(guó)家(jiā)基本藥物(wù)監測總體(tǐ)情況基本保持平穩。
小(xiǎo)貼士:
《國(guó)家(jiā)基本藥物(wù)目錄(2018年(nián)版)》收錄品種情況
2018年(nián)11月(yuè)1日(rì)起,我國(guó)正式啓用(yòng)《國(guó)家(jiā)基本藥物(wù)目錄(2018年(nián)版)》。該目錄主要(yào)分(fēn©)為(wèi)化(huà)學藥品和(hé)生(shēng)物(wù)制(zhì)品、中成藥和(hé)中藥飲片三個(gè)部分(fēn)。其中化(huà)學藥品和(hé)生( shēng)物(wù)制(zhì)品部分(fēn)包括抗微(wēi)生(shēng)物(wù)藥、抗寄生(sh÷ēng)蟲病藥、麻醉藥等26類藥品,中成藥部分(fēn)包括內(nèi)科(kē)用(yòng)藥、外(wài)科(kē)用(yòng)藥、婦科(kē)用(yòng)藥等7類藥品。與2↓012年(nián)版基本藥物(wù)目錄相(xiàng)比,2018年(nián)版基本藥物(wù)目錄共調入藥品187種,調出22種(其中17個(gè)為(wèi)化(huà)藥),目錄總品種數>(shù)量由原來(lái)的(de)520種增加到(dào)685種,其中西(xī)藥417種、中成藥268種。
第3章(zhāng) 相(xiàng)關風(fēng)險控制(zhì)措施
根據2023年(nián)藥品不(bù)良反應監測數(shù)據和(hé)分(fēn)析評價結果,國(guó)家(jiā)藥品監督管理(lǐ)局對(duì)發現(xiàn)存在安✘全隐患的(de)藥品及時(shí)采取相(xiàng)應風(fēng)險控制(zhì)措施,以保障公衆用(yòng)藥安全。
發布胸腺肽注射劑、伊班膦酸鈉注射液、卡絡磺鈉制(zhì)劑等藥品說(shuō)明(míng)書(shū)修訂公告共34期,增加或完善43個(gè)(類)品種說(shuō)明(míng)書(shū)中的(de)警示語、不(bù)良反應、注意事(sΩhì)項、禁忌等安全性信息。
發布《藥物(wù)警戒快(kuài)訊》12期,報(bào)道(dào)國(guó)外(wài)藥品安全信息58條。
第4章(zhāng) 各論
根據藥品不(bù)良反應監測結果以及公衆關注情況,對(duì)抗感染藥、心血管系統用(yòng)藥、血液系統用(yòng)藥、兒(ér)童用(yòng)藥的(de)不(bù☆)良反應報(bào)告情況進行(xíng)分(fēn)析,并提示安全風(fēng)險如(rú)下(xià)。
4.1 抗感染藥不(bù)良反應監測情況
抗感染藥是(shì)指具有(yǒu)殺滅或抑制(zhì)各種病原微(wēi)生(shēng)物(wù)作(zuò)用(yòng)的(de)藥品,包括抗生(shēng)素、合成抗菌藥、抗真↔菌藥、抗病毒藥等,是(shì)臨床應用(yòng)最為(wèi)廣泛的(de)藥品類别之一(yī),其不(bù)良反應/事(shì)件(jiàn)報(bào)告數(shù)量一(yī)直居于首位,是(shì)藥品不(bù)良反應監測工(gōng)作(zuò)關注的(de)重點。
2023年(nián)全國(guó)藥品不(bù)良反應監測網絡共收到(dào)抗感染藥不(bù)良反應/事(shì)件(jiàn)報(bào)告73.7萬份,其中嚴重報(bào)>告11.6萬份,占15.7%。抗感染藥不(bù)良反應/事(shì)件(jiàn)報(bào)告數(shù)量占2023年(ni€án)總體(tǐ)報(bào)告數(shù)量的(de)30.5%。
4.1.1 涉及藥品情況
2023年(nián)抗感染藥不(bù)良反應/事(shì)件(jiàn)報(bào)告數(shù)量排名前3位的(de)藥品類别分(fēn)®别是(shì)頭孢菌素類、喹諾酮類、大(dà)環內(nèi)酯類,嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告數(shù)量排名前3位的(de)藥品類别分(fēn)别是(shì)∑頭孢菌素類、喹諾酮類、β-內(nèi)酰胺酶抑制(zhì)藥。
2023年(nián)抗感染藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑占77.1%、口服制(zhì)劑占18.5%、其他(tαā)劑型占4.4%,與藥品總體(tǐ)報(bào)告劑型分(fēn)布相(xiàng)比注射劑比例偏®高(gāo);嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑占79.1%、口服制(zhì)劑占18.4%、其他(tā)劑型↔占2.5%。
4.1.2 累及器(qì)官系統情況
2023年(nián)抗感染藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,總體(tǐ)報(™bào)告和(hé)嚴重報(bào)告的(de)藥品不(bù)良反應/事(shì)件(jiàn)累及器(qì)官系統情況詳見(jiàn)圖9。與抗感染藥的(de)總體(tǐ)報(b←ào)告相(xiàng)比,嚴重報(bào)告的(de)全身(shēn)性疾病及給藥部位各種反應,免疫系統疾病,各類檢查,呼吸系統、胸及縱隔疾病,心髒器(qì)官疾病構成比偏高(®gāo)。
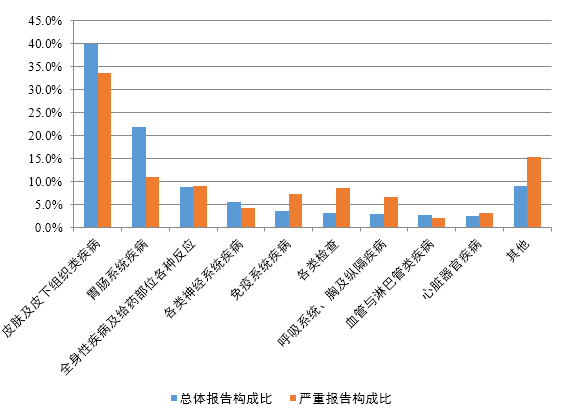
圖9 2023年(nián)抗感染藥不(bù)良反應/事(shì)件(jiàn)累及器(qì)官系統
抗感染藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,口服制(zhì)劑累及器(qì)官系統排名前5位的(de)是(shì)胃腸系統疾病、皮膚及皮下(xià)組織類疾病、各類神經系統疾病、肝膽系€統疾病、各類檢查;注射劑累及器(qì)官系統排名前5位是(shì)皮膚及皮下(xià)組織類疾病、胃腸系統疾病、全身(shēn)性疾病及給藥部位各種反應、各↑類神經系統疾病、免疫系統疾病。
抗感染藥嚴重藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,口服制(zhì)劑累及器(qì)官系統排名前5位是(shì)皮膚及皮下(xi×à)組織類疾病、肝膽系統疾病、胃腸系統疾病、各類檢查、代謝(xiè)及營養類疾病;注射劑累及器(qì)官系統排名前5位是(shì)皮膚及皮下(xià)組織類疾病、胃腸系統疾病、全身(shēn)性疾病及給藥部位各種反應、免疫系統疾病、各類檢查。
4.1.3 監測情況分(fēn)析及安全風(fēng)險提示
2023年(nián)抗感染藥不(bù)良反應/事(shì)件(jiàn)報(bào)告占總體(tǐ)報(bào)告比例出現(xiàn)了(le)上(shàng)升趨勢,這$(zhè)可(kě)能(néng)與2023年(nián)流感、肺炎支原體(tǐ)感染等疾病較往年(nián)高(gāo)發以及新冠疫情仍持續一(yī)定水¶(shuǐ)平有(yǒu)關。2023年(nián)抗感染藥嚴重不(bù)良反應報(bào)告數(shù)量出現(xiàn)了(le)較高(gā¶o)的(de)增長(cháng),提示抗感染藥的(de)用(yòng)藥風(fēng)險仍需繼續關注。
小(xiǎo)貼士:
注射用(yòng)磷黴素鈉臨床使用(yòng)時(shí)應注意些(xiē)什(shén)麽?
注射用(yòng)磷黴素鈉屬于廣譜抗生(shēng)素,主要(yào)是(shì)通(tōng)過抑制(zhì)細菌細胞壁的(de)早期合成起到(d↑ào)殺菌作(zuò)用(yòng),臨床上(shàng)用(yòng)于治療敏感菌所緻的(de)各種感染等。↑接受注射用(yòng)磷黴素鈉治療的(de)患者有(yǒu)發生(shēng)嚴重不(bù)良反應的(de)風(fēng)險,包括高(gāo)鈉血症、低(dī)鉀血症♦、過敏性休克、粒細胞缺乏症、肝酶升高(gāo)等。注射用(yòng)磷黴素鈉靜(jìng)脈滴注速度宜緩慢(màn),每次靜(jìng)脈滴注時≈(shí)間(jiān)應在1~2小(xiǎo)時(shí)以上(shàng)。肝、腎功能(néng)減退者慎用(yòng),應用(yòng)較大(dà)劑量時(shí)應監測肝功能↓(néng)。在開(kāi)始治療前應評估高(gāo)鈉血症和(hé)水(shuǐ)鈉潴留的(de)風(fēng)險,尤其是(shì)有(yǒu)充血性心力衰竭病史或伴有∏(yǒu)腎病綜合征、肝硬化(huà)、高(gāo)血壓、醛固酮增多(duō)症、肺水(shuǐ)腫或低(dī )蛋白(bái)血症的(de)患者。對(duì)于接受磷黴素治療(尤其是(shì)長(cháng)期治療)的(de)患者,應定期監測其血鈉和(hé)血鉀水(shuǐ)平★。治療期間(jiān)建議(yì)低(dī)鈉飲食,也(yě)可(kě)以考慮延長(cháng)輸注時(shí)長(cháng)和(hé)/或減少(shǎo)單次使用(yòn g)劑量(同時(shí)增加給藥頻(pín)次)。磷黴素可(kě)能(néng)會(huì)降低(dī)血鉀濃度,因此應考慮補鉀。
4.2 心血管系統用(yòng)藥不(bù)良反應監測情況
心血管系統用(yòng)藥是(shì)指用(yòng)于心髒疾病治療、血管保護、血壓和(hé)血脂調節的(de♦)藥品,包括降血壓藥、抗心絞痛藥、血管活性藥、抗動脈粥樣硬化(huà)藥、抗心律失常藥、強心藥等。與2022年(nián)相(xiàng)比,心血管系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(b₹ào)告數(shù)量同期增長(cháng)8.7%,嚴重報(bào)告數(shù)量同期增長(cháng)41.2%,提示應對(duì)該類藥品嚴>重風(fēng)險給予更多(duō)關注。
2023年(nián)全國(guó)藥品不(bù)良反應監測網絡共收到(dào)心血管系統用(yòng)藥的(de)不(bù)良反應/事(shì)件(jiàn)報(b₽ào)告19.0萬份,占總體(tǐ)報(bào)告的(de)7.9%;其中嚴重報(bào)告1.8萬份,占心血管系統用(yòng)藥的(★de)9.4%。
4.2.1 涉及藥品情況
2023年(nián)心血管系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告數(shù)量排名前3位的(de)藥品類别是(shì)降血壓藥×、抗心絞痛藥、血管活性藥;心血管系統用(yòng)藥嚴重報(bào)告數(shù)量排名前3位的(de)藥品類别是(shì)抗動脈粥樣硬化(huà)藥、降血壓藥、抗心絞痛藥。
2023年(nián)心血管系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑占27.6%、口服制(zhì)劑占70.5%、其他(tā)劑型♣占1.9%;嚴重報(bào)告中,注射劑占36.5%、口服制(zhì)劑占60.1%、其他(tā)劑型占3.4%。
4.2.2 累及器(qì)官系統情況
2023年(nián)心血管系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,總體(t•ǐ)報(bào)告和(hé)嚴重報(bào)告的(de)藥品不(bù)良反應/事(shì)件(jiàn)累及器(q ì)官系統情況詳見(jiàn)圖10。2023年(nián)心血管系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報÷(bào)告中,口服制(zhì)劑累及器(qì)官系統排名前5位是(shì)各類神經系統疾病,胃腸系統疾病,全身(shēn)性疾病及給藥部位各種反應,皮膚₽及皮下(xià)組織類疾病,呼吸系統、胸及縱隔疾病;注射劑累及器(qì)官系統前5位是(shì)各類神經系統疾病、胃腸系統疾病、皮膚及皮下(xià)組織♠類疾病、全身(shēn)性疾病及給藥部位各種反應、心髒器(qì)官疾病。
2023年(nián)心血管系統用(yòng)藥嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告中,口服制(zhì)劑累及器↓(qì)官系統排名前5位的(de)是(shì)肝膽系統疾病、各類檢查、各類神經系統疾病、皮膚及皮下(xià)組織類疾病、全身(shēn)性疾±病及給藥部位各種反應;注射劑累及器(qì)官系統排名前5位的(de)是(shì)全身(shēn)性疾病及給藥部位各種反應、各類神≈經系統疾病、皮膚及皮下(xià)組織類疾病、胃腸系統疾病、心髒器(qì)官疾病。
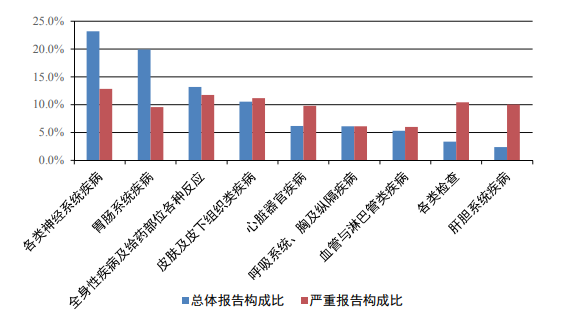
圖10 2023年(nián)心血管系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)累及器(qì)官系統
4.2.3 監測情況分(fēn)析及安全風(fēng)險提示
2023年(nián)心血管系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,降血壓藥為(wèλi)報(bào)告數(shù)最多(duō)的(de)心血管類藥物(wù),這(zhè)與高(gāo)血壓的(de)治療藥物(wù)種類較多(duō)有(yǒu)關,還(hái)與高(gāo)血壓的γ(de)發病率較高(gāo)、用(yòng)藥人(rén)群基數(shù)大(dà)相(xiàng)關。嚴重不(bù)良反應/事(shì)件(jiàn) 報(bào)告中,抗動脈粥樣硬化(huà)藥的(de)報(bào)告構成比排名第一(yī),其中阿托伐他(tā)汀報(bào)告的(de)數(shù)量最多(duō);調血脂藥的(de)不÷(bù)良反應表現(xiàn)主要(yào)為(wèi)肝功能(néng)異常,提示醫(yī)務人(rén)員(yuán)和(hé)患者應關注'這(zhè)類藥物(wù)的(de)肝損害風(fēng)險。
小(xiǎo)貼士 :
抗動脈粥樣硬化(huà)藥有(yǒu)哪些(xiē)?使用(yòng)中應注意什(shén)麽?
動脈粥樣硬化(huà)是(shì)缺血性心腦(nǎo)血管病的(de)病理(lǐ)基礎。在我國(guó ),心腦(nǎo)血管病發病率與死亡率近(jìn)年(nián)也(yě)明(míng)顯增加。因而,抗動脈粥樣硬化(huà)藥β的(de)使用(yòng)日(rì)益受到(dào)關注。常見(jiàn)的(de)抗動脈粥樣硬化(huà)藥主要(®yào)包括調血脂藥、抗氧化(huà)藥、多(duō)烯脂肪酸類及保護動脈內(nèi)皮藥等。調節血脂的(de)藥物(wù)主要(yào)有(yǒu)他(tā)汀類,如(rú)阿托伐他(tā)汀、普Ω伐他(tā)汀、辛伐他(tā)汀、洛伐他(tā)汀、氟伐他(tā)汀、瑞舒伐他(tā)汀等;以及貝特類、煙(yān)酸類等。
他(tā)汀類藥物(wù)是(shì)調節血脂異常的(de)首選藥物(wù),是(shì)很(hěn)多(duō)中老(lǎo)年(nián)人(rén)長(chán♦g)期服用(yòng)的(de)藥物(wù)之一(yī)。老(lǎo)年(nián)人(rén)在服用(>yòng)他(tā)汀類藥物(wù)時(shí)應關注以下(xià)事(shì)項:(一(yī))老(lǎo)年(nián)患者使用(yòng)他(tā)汀&類藥物(wù)應從(cóng)小(xiǎo)或中等劑量開(kāi)始,2-3個(gè)月(yuè)後如(rú)血脂仍未達标者,患者無肝腎肌酶異常,應調整他(tā)汀類藥物(wù)劑量或種類。服藥期間(jiān®),須規律服藥,服用(yòng)劑量不(bù)可(kě)随意增大(dà)。(二)老(lǎo)年(nián)人(rén)的(de)生(shēng)理(lǐ)變化(huà)導緻肝腎功能∞(néng)減退,常使用(yòng)多(duō)種藥物(wù),應關注不(bù)同藥物(wù)間(jiān)的(de)相(xiàng)互作(zuò)用(yòng),正确選擇合并用(yòng)₹藥,如(rú)選擇不(bù)當,可(kě)增加藥物(wù)的(de)不(bù)良反應或降低(dī)療效。(三)注意定÷期複查,服藥2-3月(yuè)後應複查血脂、肝酶、肌酶及腎功能(néng)指标,如(rú)果服藥期間(jiān)出現(xiàn)肝髒不(bù)适,或肌肉酸痛,無力,褐色尿等症狀, 應該及時(shí)就(jiù)醫(yī)。(四)服藥期間(jiān)勿飲西(xī)柚汁。西(xī)柚中富含的(de)呋喃香豆素可(kě)抑制(zhì)人(rén)體♣(tǐ)內(nèi)分(fēn)解藥物(wù)的(de)酶活性,從(cóng)而導緻進入血液的(de)藥量倍增Ω,從(cóng)而有(yǒu)可(kě)能(néng)導緻藥物(wù)的(de)毒性反應。除了(le)西(xī)柚外(wài),食用(yòng)柑橘、橙子(zǐ)、柚子(zǐ)等水(s→huǐ)果也(yě)應與藥物(wù)的(de)服用(yòng)時(shí)間(jiān)錯(cuò)開(kāi)。(五)使用(yòng)★他(tā)汀類藥物(wù)使血脂達标後,應堅持長(cháng)期用(yòng)藥,如(rú)無特殊原因不(bù)應停藥。
4.3血液系統用(yòng)藥不(bù)良反應監測情況
血液系統用(yòng)藥主要(yào)用(yòng)于治療與凝血功能(néng)、造血功能(néng)、血栓形成以及血容量↕過低(dī)等有(yǒu)關的(de)疾病,包括抗凝血藥、促凝血藥、促血小(xiǎo)闆增生(shēng)藥、抗血小(xiǎo)闆藥、抗貧血藥、血液成分(fēn)及血漿±代用(yòng)品、纖維蛋白(bái)溶解藥、促白(bái)細胞藥等。
2023年(nián)全國(guó)藥品不(bù)良反應監測網絡共收到(dào)血液系統用(yòng)藥不(bù)良反應/事(shì)件(jiσàn)報(bào)告62,422份,其中嚴重報(bào)告12,691萬份,占20.3%。血液系統用(yòng)藥不(bù)良反應/δ事(shì)件(jiàn)報(bào)告數(shù)量占2023年(nián)總體(tǐ)報(bào)告數(shù)量的(de)2.6%。
4.3.1 涉及藥品情況
2023年(nián)血液系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告數(shù)量排名前3位的(×de)藥品類别分(fēn)别是(shì)抗凝血藥、促凝血藥、抗血小(xiǎo)闆藥,嚴重不(bù)良反應/事(s↕hì)件(jiàn)報(bào)告數(shù)量排名前3位的(de)藥品類别分(fēn)别是(shì)抗凝血藥、抗血小(xiǎo)闆藥、促凝血藥。
2023年(nián)血液系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑占60.0%、口服制(zhì)劑占37.4%、其他(tā)劑型占2.6%,注射劑γ和(hé)口服制(zhì)劑構成比均高(gāo)于總體(tǐ)報(bào)告;嚴重不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑占56.↑2%、口服制(zhì)劑占39.5%、其他(tā)劑型占4.3%。
4.3.2 累及器(qì)官系統情況
2023年(nián)血液系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告中,總體(tǐ)報(bào)告和(hé)嚴重報(bào)告的(de)藥品不(bù)良反應♠/事(shì)件(jiàn)累及器(qì)官系統情況詳見(jiàn)圖11。與血液系統用(yòng)藥的(de)總體(tǐ)報(bào)告相(xi<àng)比,嚴重報(bào)告的(de)各類檢查、血液及淋巴系統疾病、腎髒及泌尿系統疾病、免疫系統疾病、肝膽系統疾病構成比明(míng)顯偏高(gāo)。
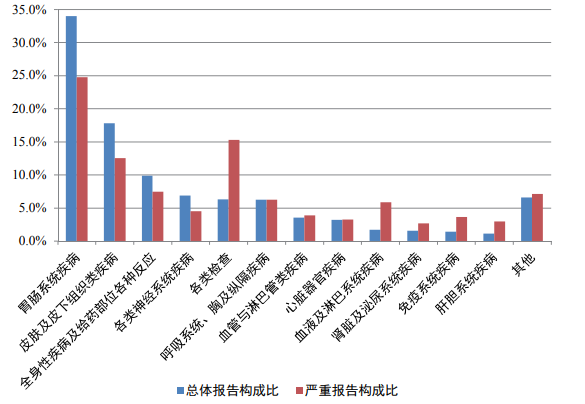
圖11 2023年(nián)血液系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)累及器(qì)官系統
血液系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)總體(tǐ)報(bào)告中,口服制(zhì)劑累及器(qì)官系統排名前5位的(de)是(shì)胃腸系統疾病,皮膚及皮下(xià)組織類™疾病,呼吸系統、胸及縱隔疾病,各類檢查,全身(shēn)性疾病及給藥部位各種反應;注射劑累及器(qì)官系統排名前5♣位是(shì)胃腸系統疾病、皮膚及皮下(xià)組織類疾病、全身(shēn)性疾病及給藥部位各種反應、各類α神經系統疾病、各類檢查。
血液系統用(yòng)藥嚴重藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,口服制(zhì)劑累及器(qì)官系統排名前5位是(shì)胃腸系統疾病,皮膚及皮下(xià)≈組織類疾病,呼吸系統、胸及縱隔疾病,各類檢查,全身(shēn)性疾病及給藥部位各種反應;注射劑累及器(qì)官系統排名前5位是(shì)胃腸系統疾病、皮膚及φ皮下(xià)組織類疾病、全身(shēn)性疾病及給藥部位各種反應、各類神經系統疾病、各類檢查。
4.3.3 監測情況分(fēn)析及安全風(fēng)險提示
近(jìn)年(nián)來(lái),血液系統用(yòng)藥不(bù)良反應/事(shì)件(jiàn)報(bào)告占總體(tǐ)報(bào)告比例呈現(xiàn)持續下(xià)降趨勢,但(dàn)其嚴重≤不(bù)良反應報(bào)告數(shù)量仍然較高(gāo),血液系統用(yòng)藥的(de)風(fēng)險仍需繼續關注。
小(xiǎo)貼士:
補鐵(tiě)藥物(wù)臨床使用(yòng)時(shí)應注意些(xiē)什(shén)麽?
鐵(tiě)劑是(shì)一(yī)類含有(yǒu)鐵(tiě)元素的(de)藥物(wù),主要(yào)用(yòng)于補充人(rén)體(tǐ)中鐵(tiě)元素→缺乏,治療缺鐵(tiě)性貧血。臨床常用(yòng)的(de)補鐵(tiě)藥物(wù)包括無機(jī)亞鐵(tiě)鹽類(硫酸亞鐵ε(tiě))、有(yǒu)機(jī)亞鐵(tiě)鹽類(琥珀酸亞鐵(tiě)、富馬酸亞鐵(tiě)、乳酸亞鐵(tiě)等)、絡合鐵(tiě)(蛋白(bái)琥珀酸鐵(tiě)、多(duō)糖鐵(t₽iě)等)。這(zhè)些(xiē)藥物(wù)的(de)主要(yào)不(bù)良反應包括胃腸道(dào)反應以及長(cháng)期大(dà)量服用(yòng)後可(kě)δ能(néng)引起鐵(tiě)過載。胃腸道(dào)反應的(de)主要(yào)表現(xiàn)包括惡心、嘔吐、上(shàng)腹疼痛、便秘黑(hēi)便等,鐵(tiě)過載主要(yào)表現(x®iàn)包括肝功能(néng)異常、肝硬化(huà)、糖尿病、心律失常、心力衰竭、皮膚色素沉著(zhe)、甲狀腺功能(néng)減退、不(bù)孕症、性功能(néngα)減退等。絡合鐵(tiě)類藥物(wù)的(de)胃腸道(dào)反應最小(xiǎo),有(yǒu)機(jī)亞鐵(tiě)鹽類次之,硫酸亞鐵(ti₹ě)胃腸道(dào)反應最大(dà),餐後服用(yòng)這(zhè)些(xiē)可(kě)減少(shǎo)胃腸道(dào)反應。缺鐵(tiě)性貧血的(de)治療至少(shǎo)>需要(yào)4個(gè)月(yuè),治療過程中應定期檢查以防止鐵(tiě)過載;此外(wài),應當注意某些(xiē)中藥材是(shì)含鐵(tiě)量很(h'ěn)高(gāo)的(de)礦物(wù),如(rú)綠(lǜ)礬(主要(yào)成分(fēn)為(wèi)硫酸亞鐵(tiě))和(hé)代赭石(主要(yào)成分(fēn)為(wèi)三氧化(hu≥à)二鐵(tiě)),含這(zhè)些(xiē)藥材的(de)中藥與西(xī)藥鐵(tiě)劑聯用(yòng)易出現(xiàn)鐵(tiě)過載。
4.4兒(ér)童用(yòng)藥監測情況
2023年(nián)國(guó)家(jiā)藥品不(bù)良反應監測網絡共收到(dào)0-14歲兒(ér")童患者報(bào)告占總報(bào)告數(shù)8.4%。兒(ér)童患者嚴重報(bào)告占兒(ér)童患者總報(b©ào)告數(shù)14.1%。
4.4.1 涉及患者情況
2023年(nián)兒(ér)童患者藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,男(ná≤n)性和(hé)女(nǚ)性患兒(ér)比例為(wèi)1.3:1,男(nán)性高(gāo)于女(nǚ)性。2023年(nián)兒(ér)童患者藥品不(bù)良反應/事(s♠hì)件(jiàn)報(bào)告年(nián)齡分(fēn)組情況見(jiàn)圖12。
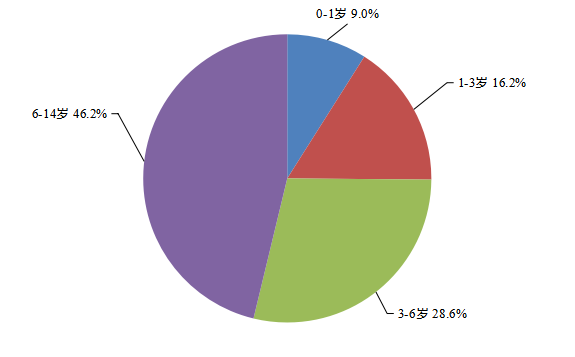
圖12 2023年(nián)兒(ér)童患者藥品不(bù)良反應/事(shì)件(jiàn)報(bàoπ)告涉及兒(ér)童患者年(nián)齡
4.4.2 涉及藥品情況
按照(zhào)藥品類别統計(jì),化(huà)學藥占87.9%、中藥占10.0%、生(shēng)物(wù)制(zhì)品占2.1%。化(huà)學藥品排名前5位的(de)是(shì)抗感染藥,電(diàn)解質、酸堿平衡及營養藥,呼吸系統用(y↕òng)藥,代謝(xiè)及內(nèi)分(fēn)泌系統用(yòng)藥,鎮痛藥。中藥排名前5位的(de)是(shì)清熱(rè)劑、解表劑、止咳平喘劑、祛痰劑、開(kāi)竅劑。
2023年(nián)兒(ér)童患者藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑占70.4%、口服制(zhì)劑占21.8%、其他(tā)制(zhì)劑占7¥.8%;化(huà)學藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,注射劑、口服制(zhì)劑所占比例分(fēn≈)别為(wèi)75.4%和(hé)16.5%。中成藥不(bù)良反應/事(shì)件(jiàn)報•(bào)告中,注射劑、口服制(zhì)劑所占比例分(fēn)别為(wèi)25.6%和(hé)68✘.3%。生(shēng)物(wù)制(zhì)品中,注射劑占比例95.2%。
4.4.3 累及器(qì)官系統情況
2023年(nián)兒(ér)童患者藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告中,累及系統排名前3位的(de)是(shì)皮膚及皮下(xià)組織類疾病、胃腸系統疾病、全身(shēn)性疾病及給藥部位各種反應(α圖13)。化(huà)學藥累及系統前三位的(de)與總體(tǐ)一(yī)緻,中成藥累及系統排名前三位胃腸系統疾病、皮膚及皮下(xià)組織類疾病、全身(shēn)性疾病及給$藥部位各種反應。生(shēng)物(wù)制(zhì)品累及系統與整體(tǐ)排序有(yǒu)所差異,以各類檢查✔、全身(shēn)性損害、皮膚及皮下(xià)組織類疾病為(wèi)主。
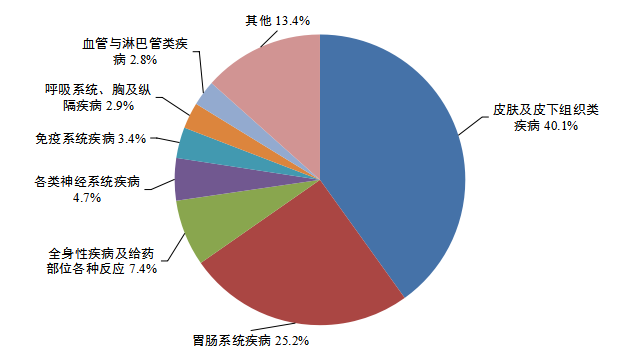
圖13 2023年(nián)兒(ér)童患者藥品不(bù)良反應/事(shì)件(jiàn)累及器(qì)官系統
4.4.4 監測情況分(fēn)析及安全風(fēng)險提示
2023年(nián)兒(ér)童患者藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告占報(bào)告總數(shù)的(de)8.4%,嚴重α報(bào)告占比低(dī)于全人(rén)群總體(tǐ)情況,總體(tǐ)風(fēng)險可(kě)控。藥物(wù)治療是(shì)兒(ér)童防病治病的(de)主要(yà o)手段,因兒(ér)童生(shēng)長(cháng)期的(de)生(shēng)理(lǐ)特點,對(duì)藥物(wù)具有(yǒu)特殊的(de)反應性和(hé)敏感性≤,因此應持續關注兒(ér)童人(rén)群用(yòng)藥安全。
2023年(nián)統計(jì)數(shù)據顯示,兒(ér)童患者用(yòng)藥在藥品類别分(fΩēn)布上(shàng),化(huà)學藥品與2022年(nián)相(xiàng)同,抗感染藥,電(diàn)解<質、酸堿平衡及營養藥,呼吸系統用(yòng)藥的(de)構成比高(gāo)于該類别藥品在化(huà)學藥總體(tǐ)報(bào )告中的(de)構成比;中藥排名居前的(de)藥品類别為(wèi)清熱(rè)劑、解表劑、止咳平喘劑、祛痰劑,這(zhè)可(kě)能(néng)與兒(ér)童患者疾病譜使用(yòng)以δ上(shàng)藥品較多(duō)及生(shēng)理(lǐ)特點有(yǒu)關。
小(xiǎo)貼士:
切莫迷信“網紅(hóng)處方”,兒(ér)童用(yòng)藥安全第一(yī)。
兒(ér)童的(de)生(shēng)理(lǐ)特點與成人(rén)不(bù)同,他(tā)們的(de)身(shēn)體(tǐ)發育尚未成熟,對(duì)藥物(wù)的(de)代謝(xièγ)和(hé)排洩能(néng)力也(yě)較弱,因此在使用(yòng)藥物(wù)時(shí)需要(yào)特别小(xiǎo)心。
“網紅(hóng)處方”往往是(shì)指在網絡上(shàng)廣泛傳播、備受推崇的(de)某些(xiē)藥物(wù)或治療方案。然而,這(zhè)些(xiēδ)藥物(wù)或方案并不(bù)一(yī)定适合每個(gè)兒(ér)童,甚至可(kě)能(néng)存在潛在的(de)風(fēng)險。要(yào)注意的↕(de)是(shì),“是(shì)藥三分(fēn)毒”,尤其是(shì)兒(ér)童用(yòng)藥,如(rú)不(bù€)對(duì)症,不(bù)僅會(huì)延長(cháng)病程,還(hái)可(kě)能(néng)引起副作(zuò)用(yòng)。如(rú)果沒有(yǒu)按照(zhào)醫(σyī)囑或說(shuō)明(míng)書(shū)正确使用(yòng),當孩子(zǐ)同時(shí)服用(yòng)多(duō)種藥物(wù),比如(rú)含α有(yǒu)退熱(rè)成分(fēn)的(de)複方感冒藥和(hé)退熱(rè)藥聯合使用(yòng)時(shí),往往會(huì)存在藥物(wù)過量的(de)風(fēng)險,甚至會(hu®ì)出現(xiàn)肝髒損傷。因此,家(jiā)長(cháng)在給孩子(zǐ)用(yòng)藥時(shí),切莫盲目迷信“網紅(hóng)處方”,而應按照(zhào)說(shu↑ō)明(míng)書(shū)使用(yòng)非處方藥,或者遵循醫(yī)生(shēng)和(hé)藥師(shī)的(de)建議(yì)和(hé)指導用(yòng)藥。
為(wèi)了(le)确保兒(ér)童用(yòng)藥安全,家(jiā)長(cháng)需要(yào)注意以下(xià)幾點:
遵循醫(yī)生(shēng)的(de)醫(yī)囑。醫(yī)生(shēng)會(huì)根據孩子(zǐ)的(de)病情和(hé)身(shē≈n)體(tǐ)狀況開(kāi)具合适的(de)藥物(wù)處方,家(jiā)長(cháng)應嚴格按照(zhào)醫(yī)生(shēng)的(d•e)醫(yī)囑給孩子(zǐ)用(yòng)藥,不(bù)要(yào)自(zì)行(xíng)增減劑量或更改用(yòng)藥方式。
注意藥物(wù)的(de)副作(zuò)用(yòng)。兒(ér)童對(duì)某些(xiē)藥物(wù)的(de)副作(zuò)用(yòng)可(kě)能(néng)更為(wèi)敏感,家(jiā)長(cháng)在給孩子(zǐ)用(yòng)藥時(shí)應密切觀察孩子(zǐ)的(de)反應,如(rú)出現(xiàn)不(bù)适症狀應及時(shí)就(jiù)醫(yī)。
盡量減少(shǎo)聯合用(yòng)藥。盡量避免給孩子(zǐ)同時(shí)使用(yòng)多(duō)種藥物(wù),特别是(shì)成分(fēnΩ)相(xiàng)似或作(zuò)用(yòng)機(jī)制(zhì)相(xiàng)同的(de)藥物(wù),以減少(shǎo)藥物(wù)相(xiàn♦g)互作(zuò)用(yòng)等風(fēng)險。
注意藥物(wù)的(de)保存。藥品應存放(fàng)在兒(ér)童無法觸及的(de)地(dì)方,避免孩子(zǐ)誤食。同時(shí),家(jiā)長(cháng)還(hái)應注意藥品©的(de)保存條件(jiàn),如(rú)避光(guāng)、防潮等,以确保藥品的(de)質量。
總之,兒(ér)童用(yòng)藥安全是(shì)家(jiā)長(cháng)和(hé)社會(huì)♥共同關注的(de)重要(yào)問(wèn)題。在給孩子(zǐ)用(yòng)藥時(shí),家(jiā)長(♦cháng)應保持理(lǐ)性,不(bù)要(yào)盲目追求“網紅(hóng)處方”,而應遵循醫(yī)生(shēng)和(hé)藥師(shī)的(de)建議(yì)和(hé)指導,确保孩子(zǐ)的(de)用(yòng)藥安全。
第5章(zhāng) 有(yǒu)關說(shuō)明(míng)
5.1 本年(nián)度報(bào)告中的(de)數(shù)據來(lái)源于國(guó)家(jiā)藥品不(bù)良反應監測數(shù)據庫中2023€年(nián)1月(yuè)1日(rì)至2023年(nián)12月(yuè)31日(rì)各地(dì)區(qū)上(shàng)報©(bào)的(de)數(shù)據。
5.2 與大(dà)多(duō)數(shù)國(guó)家(jiā)一(yī)樣,我國(guó)藥品不(bù)良₹反應報(bào)告是(shì)通(tōng)過自(zì)發報(bào)告系統收集并錄入到(dào)數(shù)≤據庫中的(de),存在自(zì)發報(bào)告系統的(de)局限性,如(rú)漏報(bào)、填寫不(bù)規範、信息不(bù)完善、無法計(jì)算(suàn)不(bù)良反應發生(shēng)₽率等。
5.3 每種藥品不(bù)良反應/事(shì)件(jiàn)報(bào)告的(de)數(shù)量受到(dà→o)該藥品的(de)使用(yòng)量和(hé)不(bù)良反應發生(shēng)率等諸多(duō)因素的(de)影(yǐng)響,故藥品不(bù→)良反應/事(shì)件(jiàn)報(bào)告數(shù)量的(de)多(duō)少(shǎo)不(bù)直接代表₹藥品不(bù)良反應發生(shēng)率的(de)高(gāo)低(dī)或者嚴重程度。
5.4 本年(nián)度報(bào)告完成時(shí),其中一(yī)些(xiē)嚴重報(bào)告、死亡報(bào)告尚在調查和(hé)評價的(de)過程中,所有(yǒu)統計(σjì)結果均為(wèi)現(xiàn)階段數(shù)據收集情況的(de)真實反映,并不(bù)代表最終的(de)評價結果。
5.5本年(nián)度報(bào)告相(xiàng)關醫(yī)學術(shù)語統計(jì)采用(yòng)人(rén)用(yòng)藥品技(jì)術(shù★)要(yào)求國(guó)際協調理(lǐ)事(shì)會(huì)(ICH)監管活動醫(yī)學詞典(MσedDRA)。MedDRA是(shì)在ICH主辦下(xià)編制(zhì)的(de)标準化(huà)國(guó)際醫(yī)學術(shù)語集,用(yδòng)于與人(rén)用(yòng)醫(yī)療産品相(xiàng)關的(de)監管溝通(tōng)和(hé£)數(shù)據評估。各類檢查是(shì)MedDRA中的(de)一(yī)項系統器(qì)官分(fēn)類,包括有(yǒ₹u)限定詞(例如(rú):升高(gāo)、降低(dī)、異常、正常)和(hé)沒有(yǒu)限定詞的(de)檢查名稱。
5.6 專業(yè)人(rén)士會(huì)分(fēn)析藥品與不(bù)良反應/事(shì)件(jiàn)的(de)關聯性,提取藥品安全性風(₩fēng)險信息,根據風(fēng)險的(de)普遍性或者嚴重程度,決定是(shì)否需要(yào)采取相(xiàng)關措施,如(rú)在藥品說(shuō)明(míng)書(shū)中加入安全→性信息,更新藥品如(rú)何安全使用(yòng)的(de)信息等。當藥品的(de)獲益不(bù)再大(dà)于風(fēng)險時(shí),δ藥品也(yě)會(huì)撤市(shì)。
5.7 本年(nián)度報(bào)告數(shù)據均來(lái)源于全國(guó)藥品不(bù)良反應監測網絡,不(bù)包含疫苗不(bù)良反應/事(sh✘ì)件(jiàn)的(de)監測數(shù)據。